Abschied von Illusionen
Plädoyer für eine wissenschaftlich fundierte Herzmedizin
Glaubt man den Hochglanzprojekten, mit denen die Kardiologie ihre Produkte (Katheter, Stent, Bypass, Klappenersatz) präsentiert, dann handelt es sich um eine Wunderwelt ohne Probleme. Doch das geht an der Realität vorbei: Herzkatheter und Stents bieten keinen Schutz vor einem Herzinfarkt und können das Leben der herzkranken Patienten nicht verlängern. Das haben alle großen Studien gezeigt, und die brandaktuelle Studie, ISCHEMIA, hat diese Ergebnisse voll bestätigt. In diesem Statement erläutere ich, warum Bypass, Stent und Herzkatheter zwangsläufig scheitern müssen und warum es dringend notwendig ist, sich von diesen Eingriffen mitsamt ihren Illusionen zu verabschieden. Eine grundlegende Neuorientierung ist überfällig. Die Herzpatienten haben eine sinnvollere und bessere Behandlung verdient.
In ISCHEMIA wurden über 5000 Patienten mit schweren Kranzgefäßveränderungen in 10 kardiologischen Spitzenzentren rund um den Globus einbezogen. Alle Patienten erhielten eine medikamentöse Therapie nach derzeitigem Standard. Bei der Hälfte der Patienten wurde zusätzlich ein Herzkatheter gelegt und bei diesen Patienten folgte anschließend ein Eingriff an den Kranzgefäßen: Zwei Drittel erhielten Stents, ein Drittel wurde Bypass-operiert. In der Vergleichsgruppe, den anderen 2500 Patienten mit vergleichbar schweren Kranzgefäßverengungen, wurde kein Katheter gelegt, man beließ es bei den Medikamenten.
Ende 2019 wurden die Ergebnisse auf dem Jahreskongress der American Heart Association vorgestellt. Die Zahl der Todesfälle war nach 3 ½ Jahren Laufzeit in beiden Gruppen absolut identisch. Die Anzahl der Herzinfarkte zeigte ebenfalls keine Unterschiede. Herzkatheter, Stent und Bypass-OP bieten Herzpatienten keinen wirksamen Schutz und sind zudem mit nicht unerheblichen Schäden belastet.
Die Kranzgefäßverengungen, die koronaren Stenosen, gelten bekanntlich als das entscheidende Übel. Das große Versprechen der modernen Kardiologie basiert auf der Beseitigung bzw. Ausschaltung der Stenosen. Geradezu reflexartig wird zum Herzkatheter gegriffen, wenn eine Kranzgefäßverengung vermutet wird.
In den folgenden Ausführungen gehe ich zunächst der Frage nach, inwieweit schwere koronare Stenosen tatsächlich ein Übel sind. Ich konfrontiere Aufnahmen aus Herzkatheter-Filmen mit korrespondierenden anatomischen Bildern. In dieser Gegenüberstellung wird der völlig überraschende Befund für jedermann erkennbar: Schwere Kranzgefäßverengungen sind überhaupt kein Hindernis für den Blutstrom. Der koronare Blutfluss wird durch schwere und schwerste Stenosen nicht aufgehalten. Denn – wie die anatomischen Befunde zeigen – die Natur weiß sich selber zu helfen. Stent und Bypass zielen ins Leere. Sie können an der koronaren Durchblutung nichts verbessern.
Danach gebe ich eine Übersicht über die wichtigsten Studien der letzten 20 Jahre zur Wirksamkeit von Katheter und Stent bei Herzpatienten. Diese „Meilensteine“ sind die wissenschaftlichen Zeugnisse für die Unwirksamkeit dieser Eingriffe. Sie belegen in exakten Zahlen, dass Katheter und Stent keinen Schutz vor einem Herzinfarkt bieten und kein Leben verlängern.
Abschließend skizziere ich ein Konzept für eine grundlegende Neuorientierung in der Behandlung von Herzpatienten. Ein Paradigmenwechsel ist überfällig. Die moderne Herzmedizin folgt nicht den gesicherten wissenschaftlichen Erkenntnissen. Eine wissenschaftlich fundierte Herzmedizin wird sich von Katheter, Stent und Bypass verabschieden. Neue Wege müssen sich auftun.
Katheter gegen Anatomie
Stenosen im Herzkatheter-Film
Eine Herzkatheter-Untersuchung wird stets gefilmt und so der Zustand der Kranzgefäße, ob frei durchgängig oder mehr oder weniger stark verengt, dokumentiert. In den folgenden Filmsequenzen werden durch das Einspritzen von Kontrastmittel über einen Herzkatheter schwere Kranzgefäßverengungen sichtbar. Diese kurzen Filme geben Gelegenheit, die Auswirkungen einer Stenose auf den koronaren Blutfluss zu studieren.
Auf einem Eingangsbild ist stets die durch einen Pfeil markierte Stenose zu erkennen. Danach sehen Sie das gleiche Bild ohne Pfeil, damit sich das Auge in die vorliegenden Verhältnisse einsieht. Dann folgt der Katheterfilm, zweimal nacheinander in Echtzeit und schließlich noch zweimal in Zeitlupe.
Es handelt sich um eine hochgelegene mindestens 90%ige Stenose einer der beiden linken Kranzarterien („LAD“). Die linke wie die rechte Kranzarterie haben ihren Ursprung in der Aorta. Die linke zweigt sich nach kurzem Verlauf, dem sogenannten Hauptstamm, in zwei große Gefäße auf. Auf dem Eingangsbild mit und ohne Pfeil ist ganz links oben der gebogene Katheter und im Anschluss an die Katheterspitze der mit Kontrastmittel gefüllte Hauptstamm gut zu erkennen. Die schwere Stenose liegt kurz hinter der Aufzweigung in zwei große Gefäße.
Die Zeitlupenversion dauert in Echtzeit genau eine Sekunde und veranschaulicht die Gefäßfüllung hinter der Stenose während der ersten Sekunde. Dieser Film zeigt einen typischen Ablauf: In Anwesenheit einer schweren Stenose füllt sich die Kranzarterie hinter der Stenose vollständig und ohne jede Verzögerung. Der hochgradige Gefäßengpass stellt kein Hindernis für den koronaren Blutfluss dar.
Es folgen zwei weitere Beispiele. Im nächsten Film sieht man zunächst zwei aufeinanderfolgende schwere Stenosen im mittleren Abschnitt der anderen linken Kranzarterie („RCX“). Dann folgt eine 99%ige Stenose der rechten Koronararterie ebenfalls mehr im mittleren Gefäßverlauf. Der Ablauf der Filme ist identisch mit dem ersten Mal.
Die schweren Stenosen sind klar zu erkennen und genauso deutlich ist zu verfolgen, wie die markanten Engpässe überhaupt kein Hindernis für den Blutstrom im Koronargefäß darstellen. Eine schwere koronare Stenose lässt durchaus noch einen gewissen Blutstrom passieren. Es wäre jedoch, nach allgemeinem Verständnis, zu erwarten, dass sich das Gefäß hinter einer Stenose mit deutlich erkennbarer Verzögerung und auch wesentlich schwächer füllt als vor dem Hindernis. Das ist nicht der Fall. Der Abschnitt des Kranzgefäßes hinter dem Engpass füllt sich kräftig und ohne jede Verzögerung.
Diese drei exemplarischen Beispiele lassen sich endlos fortsetzen. Ob hochgelegen oder im mittleren Abschnitt, in einer der linken oder der rechten Koronararterie, in Haupt- oder Nebenästen, schwere und schwerste Kranzgefäß-Stenosen stellen kein Hindernis für den Blutfluss dar. Dies ist in geraffter Form noch einmal dem nächsten Film mit vier weiteren Beispielen zu entnehmen.
Die anatomische Wahrheit
Diese Bilder widersprechen der herrschenden Logik, nach der eine schwere Kranzgefäß-Stenose ein Durchblutungshindernis darstellt. Hier hilft die Wissenschaft weiter. In der anatomischen Forschung gelingt es, mit der Methode der Plastination die Herzdurchblutung sichtbar zu machen. So konnte erkannt werden, dass der Herzmuskel von einem umfassenden Gefäßnetz durchzogen ist, das alle Abschnitte des Herzens miteinander verbindet.
Die beiden folgenden Bilder – das Herz einmal von vorn, einmal von hinten – geben einen Eindruck von der realen Gefäßversorgung des Herzmuskels. Alle weiteren Abbildungen wurden ebenfalls von Professor Giorgio Baroldi, einem Mailänder Anatom und Pathologen, erstellt.
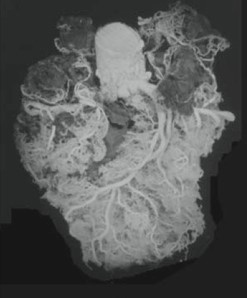
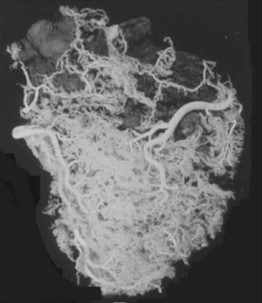
Abb.1: Gefäßversorgung eines gesunden Herzen, von vorn (oben) und von hinten gesehen (unten) – Darstellung mittels Plastination
Im Fall eines Kranzgefäßverschlusses, wie in unseren Filmen gezeigt, ergibt sich folgendes Bild (Abb.2).
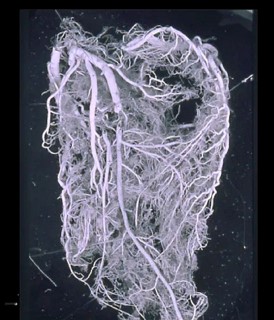
Abb.2: Gefäßversorgung bei einem Verschluss der linken vorderen Kranzarterie – mittels Plastination
Diese Bilder machen deutlich, wieso sich der Blutfluss im Kranzgefäß nicht durch eine Verengung oder einen vollständigen Verschluss aufhalten lässt. Es stehen unzählige kleine Gefäßverbindungen zwischen den Arterien zur Verfügung, die das Blut um den Engpass herumleiten. Die Mehrzahl dieser Umgehungsgefäße oder „Kollateralen“ haben ein zu feines Kaliber, um auf den Katheter-Bildern mit der derzeitigen räumlichen Auflösung erkannt zu werden. Deshalb erscheinen sie nicht oder bestenfalls als unscharfe Andeutung auf den Katheter-Filmen.
Vor Stent, nach Stent
Es folgen 3 Beispiele von schweren koronaren Stenosen, einmal vor Stent und einmal nach Beseitigung der Stenose und Platzieren eines Stents. Der erste Teil der Filme bezieht sich auf die Verhältnisse vor Stent, der zweite Teil auf die gleiche Arterie nach Stent.
Vor Stent zeigt sich auch in diesen Beispielen die Effektivität der Umgehungs-Kollateralen. Der Stent kann die Durchblutung offenbar nicht verbessern.
Chronischer kompletter Verschluss
Was sich auf den gezeigten zehn Beispielen in den Filmen abspielt, trifft auf schwere koronare Stenosen zu. Bei chronisch vollständig verschlossenen Kranzgefäßen sieht es anders aus. Das folgende Bild (Abb. 3) gehört zu einem Patienten, bei dem schon länger ein kompletter Verschluss einer Kranzarterie vorliegt, ohne dadurch einen Herzinfarkt ausgelöst zu haben.
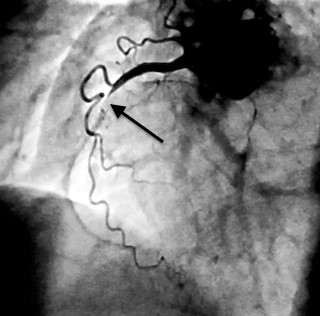
Abb.3: : Gefäßversorgung des Herzens – Darstellung mittels Herzkatheter – bei einem chronischen kompletten Verschluss der rechten Kranzarterie.
Der Gefäßverschluss ist mit einem Pfeil markiert. Unterhalb vom Verschluss erkennt man schemenhaft das Hauptgefäß, die rechte Kranzarterie. Dafür markiert sich um so deutlicher eine korkenzieherartige Kollaterale, die vor dem Verschluss abzweigt und das gleiche Muskelareal versorgt wie die Hauptarterie.
Die rechte Kranzarterie wirkt hinter dem Verschluss eher wie ein totes Gleis, transportiert aber durchaus noch Blut. Die Kollaterale übernimmt die Hauptfunktion. Nicht zu sehen sind Zuflüsse von der linken Seite, weil die linken Kranzarterien nicht gleichzeitig mit Kontrastmittel gefüllt wurden.
Wie es um die Durchblutungsverhältnisse bei einem kompletten Kranzgefäß-Verschluss in Wirklichkeit bestellt ist, ist auf den folgenden drei anatomischen Bildern gut zu erkennen.
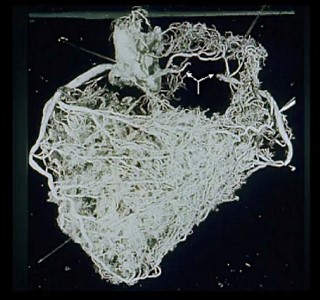
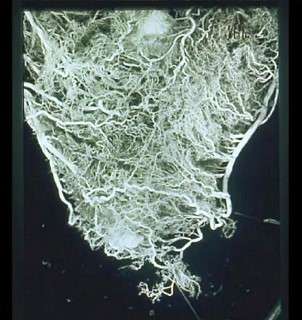
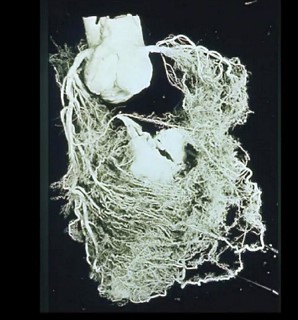
Abb.4: Gefäßversorgung des Herzens – Darstellung mittels Plastination – bei einem chronischen kompletten Verschluss der rechten Kranzarterie. Oben: rückseitige Ansicht, Mitte: vorderseitig, Unten: die Scheidewand
Es handelt sich auch hier um einen kompletten Kranzgefäßverschluss der rechten Koronararterie, im oberen Bild mit zarten Pfeilen markiert. Die umfassenden Gefäßgeflechte in der rechten Herzkammer sowie der Hinterwand der linken Herzkammer (oberes Bild), in der Vorderwand der linken Herzkammer (Mitte) und in der Kammer-Scheidewand (unteres Bild) geben einen Eindruck vom Sicherungssystem der Durchblutung des menschlichen Herzens. Unzählige Zuflüsse über feine Kollateralgefäße und auch über korkenzieherartige größere Kollateralen aus allen (!) Regionen des Herzmuskels schützen das Herz im Fall eines Kranzgefäßverschlusses.
Mit dem Herzkatheter wird davon so gut wie nichts erfasst, weil man nur die größeren gewundenen Gefäße als Kollateralen zur Kenntnis nimmt. Der überwältigende Reichtum an feineren Kollateralen wird mit der derzeitigen räumlichen Auflösung nicht erkannt und schlicht für nicht existent erklärt.
Auf dem Protokoll, das einem Patienten nach einer Katheter-Untersuchung überreicht wird und auf dem die gefundenen Verengungen und Verschlüsse eingezeichnet werden, sind Kollateralen nicht vorgesehen.
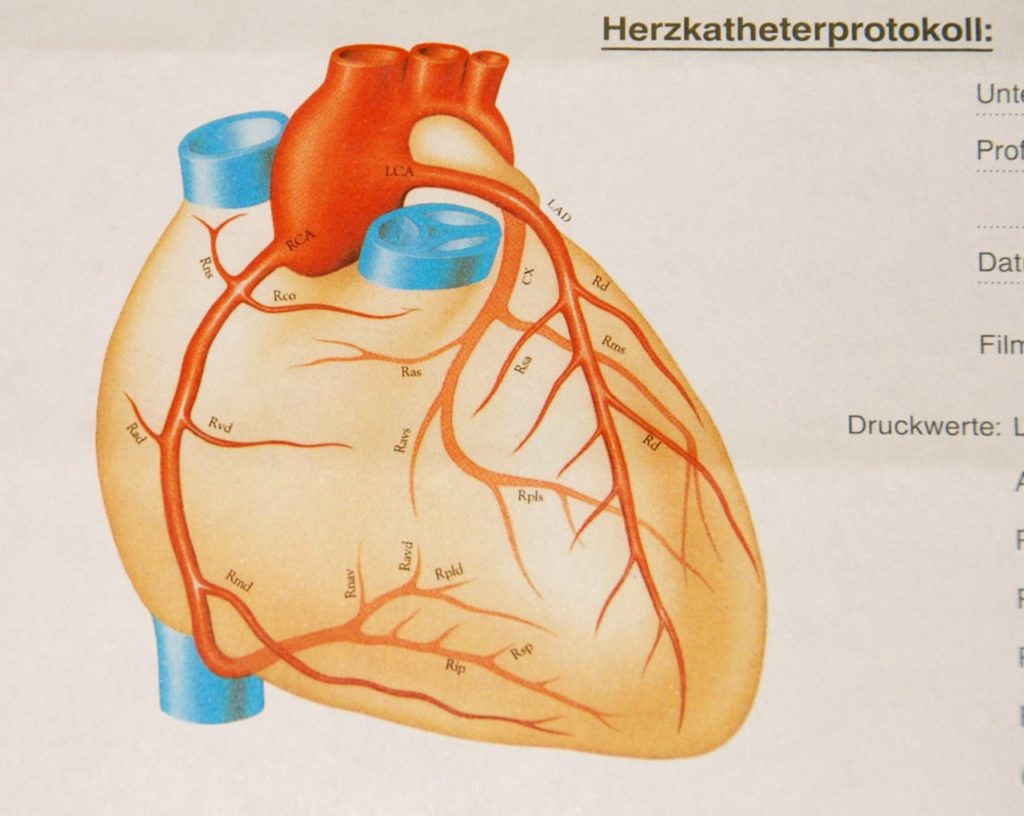
Abb.5: Skizze der Gefäßversorgung auf einem Herzkatheter-Protokoll
Eine Plaque bricht auf
Damit zu einer entscheidenden Frage: Wenn schon schwere koronare Stenosen den Blutfluss nicht beeinträchtigen, was ist, wenn sich eine Stenose durch eine aufbrechende fettreiche Gefäß-Plaque plötzlich vollständig verschließt? Entsteht dann ein Herzinfarkt?
Das umfassende Gefäßnetz, das den gesamten Herzmuskel durchzieht, ist bereits bei der Geburt nachzuweisen und schon in der Kindheit funktionsfähig. Dieses Gefäßnetz ist die Basis für die lebenslange Sicherung einer ausreichenden Durchblutung des Herzens. Immer dann, wenn sich verschließende Engpässe in den Kranzgefäßen entwickeln, was bei zahllosen westlichen Menschen der Fall ist, erweitern und verlängern sich unzählige feine Gefäße und werden dadurch, von ihrer Funktion her, zu Kollateralen. Dies geschieht proportional zum Schweregrad und zur Anzahl der schweren Stenosen.
In direkter Umgebung um eine Kranzgefäßstenose herum häufen sich die Kollateralen. Deshalb fließt das Blut so flott um alle Stenosen herum. Von anatomischer Seite ist gesichert, dass das Kaliber dieser direkten Umgehungsgefäße zusammengenommen die Größe der Restöffnung innerhalb einer Stenose weit übertrifft. Das heißt, dass das kollaterale System wesentlich mehr Blut transportiert als die Gefäßenge passieren kann. Bei einer schweren Stenose um 90%, die sich dem Auge als äußerst bedrohlich darstellt, beträgt die Transportkapazität der Umgehungs-Kollateralen ein Vielfaches der Stenose.
Was ist, wenn die restlichen 10% plötzlich wegfallen? Als anschauliches Beispiel möge Film 1 dienen. Was wäre, wenn der schmale Strich innerhalb der Stenose nicht mehr zu sehen ist? Dessen Beitrag zum koronaren Blutfluss ist wesentlich geringer als der Beitrag der nicht sichtbaren Kollateralen, die die Hauptmenge an Blut um die Stenose herumleiten. Am koronaren Blutfluss hinter dem Verschluss wird sich nichts Entscheidendes ändern.
Es ist experimentell an Herzpatienten gezeigt worden, dass ein akuter Verschluss einer linken Kranzarterie durch einen Ballonkatheter unmittelbar, innerhalb einer Minute, zu deutlichen Erweiterungen der Kollateralgefäße von der rechten Herzseite führt. Es ist davon auszugehen, dass ein plötzlicher vollständiger koronarer Gefäßverschluss über die direkten Umgehungsgefäße und über den von allen Seiten heranströmenden Blutfluss effektiv vor Schäden gesichert ist.
Das Cutoff-Phänomen
Bei größeren Herzinfarkten zeigen die Katheterbilder nicht selten einen „Cutoff“ des koronaren Blutflusses. Das folgende Bild entstammt der Herzkatheter-Untersuchung eines meiner Patienten mit einem akuten schweren Herzinfarkt. Der Fluss des Kontrastmittels bricht an einer Stelle, im Bereich einer Verengung, komplett ab.
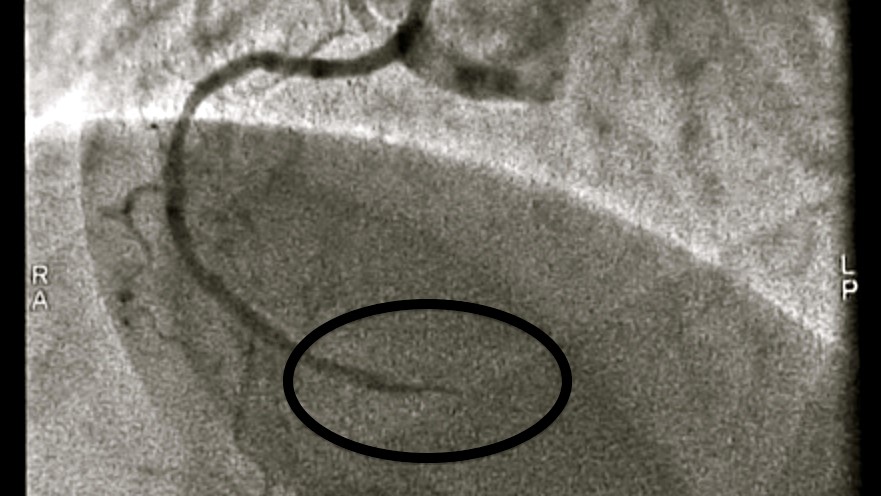
Abb.6: Cutoff-Phänomen
Nach herrschender Annahme geht man bei einem Cutoff-Phänomen davon aus, dass eine Plaque aufgebrochen ist, dass eine Thrombose das Gefäß vollständig verschlossen hat und dass dadurch ein Herzinfarkt ausgelöst wurde. Ein Cutoff widerlegt scheinbar alle Zweifel an der funktionellen Bedeutung koronarer Stenosen.
Doch man fragt sich, wo der kollaterale Blutfluss geblieben ist. Nehmen wir noch einmal das anschauliche Beispiel aus Film 1: Die Füllung des Kranzgefäßes hinter der Stenose geht zu einem kleinen Teil aufs Konto der Restöffnung und zu einem wesentlich größeren Teil aufs Konto der Kollateralen. Wenn sich die schmale Restöffnung ganz verschließt, dann wird der Blutfluss im gesamten Kranzgefäß nicht entscheidend leiden. In jedem Fall bleibt die Füllung mit Kontrastmittel hinter der Stenose deutlich erkennbar erhalten.
Warum funktionieren die Kollateralen absolut nicht mehr? Wieso soll die Entwicklung einer Thrombose im Bereich einer schweren Stenose den kompletten Ausfall der Umgehungsgefäße nach sich ziehen? Eine Analyse des Cutoff-Phänomens unter Anerkennung des kollateralen Sicherungssystems wirft unerwartete Fragen auf.
Zur Beantwortung dieser Fragen muss man sich die Freiheit nehmen, die Möglichkeit ins Auge zu fassen, dass ein Herzinfarkt unabhängig von Kranzgefäßveränderungen aus ganz anderen Gründen entstehen kann. Im dritten Abschnitts dieses Arbeitspapiers, „Die Wende“, entwickle ich in Grundzügen eine solche Möglichkeit. An dieser Stelle nur soviel: Ein Herzinfarkt wird stets durch einen akuten Durchblutungsmangel ausgelöst. Der Stopp der Durchblutung muss jedoch nicht in den drei großen, dem Herzmuskel aufliegenden Kranzgefäßen, liegen, sondern zum Stopp kann es auch in den Aufzweigungen dieser Gefäße innerhalb der Muskulatur kommen.
Übersäuerung des Herzmuskels, auf deren Ursache weiter unten eingegangen wird, führt zur Überdehnung der Muskulatur. Die überdehnten Muskelareale können im Endeffekt einen so hohen Gewebsdruck entwickeln, dass die Blutgefäße in diesem Bereich zunehmend komprimiert werden. Dadurch wird ein kleinerer oder größerer Bereich des Herzmuskels von der Blutzufuhr abgeschnitten, und es kann sich ein Herzinfarkt entwickeln. Der Auslöser für diesen Durchblutungsstopp liegt nicht in Kranzgefäß-Stenosen, sondern in Geschehnissen im Herzmuskel.
Ein Herzinfarkt, der sich unabhängig von koronaren Stenosen und Verschlüssen in der Muskulatur entwickelt, bleibt nicht ohne Konsequenzen für die koronare Durchblutung. Das Blut in der zum Infarktgebiet führenden Kranzarterie wird sich aufstauen. Im Infarktbereich selber sind die Endverzweigungen der Kranzarterie abgedrückt und auch die kleinen Kollateralen der Region sind komprimiert. Das aus der Kranzarterie anströmende Blut trifft hier auf eine Wand. In diesem Endsack des Koronargefäßes steht das Blut. Und auch in den direkten Umgehungs-Kollateralen um die Stenose herum steht das Blut. Das zum großen Teil über diese Kollateralen um die Stenosen herumgeleitete Blut erreicht nicht sein Ziel. Es ist kein Blutfluss – in die eine wie die andere Richtung – mehr möglich.
Wenn Blut nicht bewegt wird, kommt es zur Thrombose. In Höhe der Stenosen können sich Gefäßkrämpfe ausbilden. So kann es zu Einrissen der Gefäßwand im Bereich der Stenosen mit nachfolgender Thrombusbildung kommen. Das Cutoff-Phänomen findet seine schlüssige Erklärung im Aufstau des koronaren Blutflusses als Folge eines Herzinfarkts, der sich unabhängig von Gefäßprozessen primär im Herzmuskel entwickelt hat. Wenn dieser Aufstau sekundär zur Thrombusbildung führt, ergibt sich ein Cutoff-Phänomen. Weder durch die Gefäßenge noch über die rettenden Umgehungsgefäße kann sich das eingespritzte Kontrastmittel fortbewegen.
Nun zur Häufigkeit der thrombotischen Gefäßverschlüsse. Der italienische Pathologe Baroldi hat in den Siebzigern in der Universitätsklinik von Mailand in einer Serie 100 Patienten seziert, die im Verlauf eines frischen Herzinfarkts verstorben waren. Vollständige thrombotische Gefäßverschlüsse im Sinn eines Cutoff fanden sich bei 38 Patienten. Bei 62 Patienten wurde kein Gefäßverschluss angetroffen. Ein Kranzgefäßverschluss durch eine Thrombose, der Dreh- und Angelunkt in der Entstehung eines Herzinfarkts nach herrschendem Konsens, schied also bei fast zwei Drittel aller Fälle als Infarktursache aus.
Nach dieser Studie von Baroldi waren verschließende Gefäßthrombosen nur selten bei kleineren Infarkten anzutreffen, hingegen häufiger bei ausgedehnten Infarkten. Und auch: Bei Patienten, die innerhalb der ersten zwei Tage nach Infarkteintritt verstorben waren, fanden sich in 15%(!) akute thrombotische Kranzgefäßverschlüsse, bei den zwischen dem 3. und dem 10. Tag Verstorbenen waren es immerhin 50%.
Der Blutstau ist vor größeren Infarkten ausgedehnter als vor kleineren. Je länger ein Stau anhält, desto häufiger können Gefäßplaques in schweren Stenosen einreißen und zur Bildung von Thrombosen führen. Die Studie von Baroldi untermauert die Annahme, dass sich ein Infarkt primär im Herzmuskel entwickelt und dass die Veränderungen an den Stenosen, die Einrisse und Thrombosen, sekundäre Ereignisse sind.
Effektiv wirksame Stenosen?
Die Katheter-Untersuchung der Herzkranzgefäße ist diagnostisch nicht hilfreich. Sie erfasst nur randständige Aspekte der anatomischen Wahrheit. So wird die kollaterale Sicherung der Herzdurchblutung nur in Einzelaspekten erfasst. Damit können korrekte Aussagen über die wirklichen Durchblutungsverhältnisse im Herzmuskel mit der Katheter-Methode nicht gemacht werden.
Um aus diesem Dilemma herauszukommen, hat man versucht, Kriterien zu entwickeln, nach denen man annehmen kann, ob eine schwere Stenose „hämodynamisch“ wirksam ist, das heißt, ob diese Stenose tatsächlich die Herzdurchblutung behindert oder nicht. Das Druckgefälle zwischen dem Gefäßabschnitt vor und dem hinter der Stenose gilt als ein solches Kriterium. Wenn dieses Gefälle einen bestimmten Grad überschritten hat, wird eine Stenose für hämodynamisch wirksam klassifiziert.
Auch in dieser Argumentation wird das kollaterale System weitgehend ausgeblendet. Die Stenosen befinden sich in den großen Kranzarterien, die dem Herzmuskel aufliegen, d.h., die außerhalb des Herzmuskels verlaufen. Das kollaterale System agiert innerhalb der Herzmuskulatur und sorgt durch vielfältige Zuflüsse von allen Seiten für die Aufrechterhaltung einer ausreichenden Durchblutung, wie die Abbildungen zeigen. Das Druckgefälle rund um die Stenosen ist ohne Aussagekraft, weit hinter den Stenosen innerhalb der Muskulatur spielt die Musik.
In einer großen Studie (FAME II) hat man ausschließlich ausgetestete und als hämodynamisch wirksam klassifizierte Stenosen mit dem Katheter behandelt und dies mit einer rein medikamentösen Behandlung verglichen. Hinsichtlich Infarktverhütung und Lebenserwartung ergaben sich keine Unterschiede zwischen den beiden Gruppen. Es wurde deutlich: Der Katheter-Eingriff bei diesen speziellen Stenosen ergab keine Vorteile gegenüber einem Nicht-Eingriff.
Der reflektorische Griff zum Katheter führt also nicht weiter. Diese Untersuchungsmethode agiert nach dem Modus: „Man nimmt an“. Der Katheter-Reflex ist vom Augenschein diktiert und widerspricht den wissenschaftlichen Erkenntnissen.
Meilensteine
2003
Nachdem bis zum Jahr 2000 bereits Millionen an Herzkathetern geschoben und Millionen an Stents gesetzt waren, zog die weltberühmte Mayo-Klinik in den USA im Jahr 2003 eine erste grundlegende Bilanz:
+ Bei KHK-Patienten, also Patienten mit schweren koronaren Engpässen, die bei körperlicher Belastung unter Angina-pektoris-Beschwerden leiden, kann der Eingriff mit dem Ballon-Katheter die Beschwerden verringern.
+ Der Katheter-Eingriff verhütet keinen Herzinfarkt und keinen Todesfall.
+ Stents verhüten die Ausbildung einer erneuten Verengung an gleicher Stelle, senken jedoch nicht die Häufigkeit von Infarkten und Todesfällen.
Das heißt unterm Strich: Der Herzkatheter kann punkto Beschwerden, also symptomatisch, helfen. Katheter und Stent bieten aber keinen Schutz vor einem Herzinfarkt und können das Leben von Patienten mit schweren Kranzgefäßveränderungen nicht verlängern. Der Griff zum Katheter kann also nicht ursächlich helfen.
2007
In diesem Jahr erschien die COURAGE-Studie, für die etwas mehr als 2.000 Patienten mit schweren koronaren Stenosen und belastungsabhängigen Herzschmerzen in üblicher Form medikamentös behandelt wurden. Die Hälfte der Patienten wurde zusätzlich mit Katheter und Stent behandelt. Diese Studie lief über knapp 5 Jahre und wurde an 50 kardiologischen Zentren der USA und Kanada durchgeführt.
Die Zahl der Todesfälle war in beiden Gruppen, also mit und ohne Katheter-eingriff, identisch. Die Häufigkeit an Herzinfarkten und Schlaganfällen zeigte ebenfalls keine Unterschiede. Unter den Bedingungen einer üblichen medikamentösen Behandlung konnte der Einsatz von Katheter und Stent kein Leben verlängern und keinen Herzinfarkt verhindern.
Interessant ist auch, dass sich die Sterblichkeit dieser Herzpatienten, alle mit schweren koronaren Verschlüssen, mit und ohne Katheter-Eingriff in den ersten Jahren überhaupt nicht von der Normalbevölkerung unterschied – und später nur unwesentlich. Der Herzinfarkt ist nicht mehr der „Killer Nummer Eins“. Dieses Resultat der COURAGE Studie ist ein Indiz, dass das Thema Herzinfarkt künstlich überdramatisiert wird.
2016
Seit der COURAGE Studie haben sich die Stimmen in den Medien und auch unter Ärzten gemehrt, die davor warnten, dass viel zu viele Herzkatheter geschoben werden. Dabei bezieht man sich stets auf Patienten mit chronischen Belastungsbeschwerden. Bei akuten Beschwerden, bei Verdacht auf einen Herzinfarkt, galt und gilt der Katheter-Eingriff als unstrittige, weil lebensrettende Maßnahme.
Die Studien zu der Frage, ob der sofortige Griff zum Katheter bei drohendem Herzinfarkt sinnvoll ist, kamen zu unterschiedlichen Resultaten. In einigen Studien fand sich, zumindest in Untergruppen ein lebensverlängernder Effekt durch den sofortigen Katheter-Einsatz. In anderen ergab sich kein derartiger Effekt und die Schäden überwogen. Eine zusammenfassende, eine Meta-Analyse, der großen methodisch einwandfreien Studien musste her. Eine solche Meta-Analyse wurde 2016 von der Cochrane Library veröffentlicht. Die Cochrane Library ist ein von der Industrie unabhängiges Netzwerk von Ärzten und Wissenschaftlern, das für seine Objektivität bekannt ist.
Die Cochrane-Analyse der acht wichtigsten Studien ergab, dass bei drohendem Herzinfarkt der sofortige Einsatz mit Herzkatheter, Stent und auch Bypass-OP keinen lebensverlängernden Effekt gegenüber einem nicht eingreifenden, abwartenden Vorgehen hat.
Die Cochrane-Analyse ergab außerdem, dass das Risiko, im ersten Jahr nach dem Ereignis zu sterben oder einen nicht tödlichen Herzinfarkt zu erleiden, durch den frühzeitigen Einsatz eines Herzkatheters nicht gesenkt wird. Bei 6 von 100 Patienten wurde durch den Katheter-Eingriff ein Herzinfarkt ausgelöst, bei 7 von 100 kam es zu schweren Blutungskomplikationen.
Dieses vernichtende Urteil einer objektiven, nicht von industriellen Interessen gesteuerten Analyse, hat allerdings an der gängigen Praxis in den Herzkliniken nichts geändert. Jedem Patienten, bei dem der Verdacht auf einen Herzinfarkt besteht, wird vermittelt, dass ihm umgehend ein Katheter geschoben werden muss, wenn ihm sein Leben lieb ist.
Nicht nur bei Verdacht auf einen Herzinfarkt, auch bei einem bereits eingetretenen, gesicherten Infarkt, ist der Katheter-Eingriff quasi sakrosankt. Dabei ist man bemüht, nicht mehr als 90 Minuten bis zum Legen des Katheters vergehen zu lassen. Das größte Herzkatheter-Register der USA kam nach Auswertung von 100 000 Patientendaten zu dem Schluss, dass durch den frühen Katheter-Eingriff die Sterblichkeit der Patienten mit gesichertem Infarkt nicht beeinflusst wird.
Ein Herzkathetereingriff gilt heute als weitgehend risikolos. Die eingriffsbedingten Schäden des Katheters werden heute systematisch klein geredet. Das begann damit, dass man bald nach dem Jahr 2000 einen Herzinfarkt als Folge eines Kathetereingriffs neu definierte. Um verständlich zu machen, worum es dabei ging, muss etwas ins Detail gegangen werden.
In der Definition eines Herzinfarkts spielt ein bestimmter Blutwert, die sogenannte CK-MB, eine wichtige Rolle. Allgemein gilt, wenn die CK-MB erhöht ist, wird von einem Herzinfarkt ausgegangen.
Es gibt eine Obergrenze, auf Englisch „Upper Limit of Normal“ = „ULN“. Wenn der CK-Wert diese Obergrenze überschritten hat, also „größer als 1xULN“ ist, ist es ein Herzinfarkt. Bei einem Herzinfarkt als Folge des Eingriffs wurde damals jedoch auf Betreiben der Harvard University die Obergrenze auf „größer als 3xULN“ heraufgesetzt. Alle Infarkte als Folge eines Katheter-Eingriffs bis zu dieser Grenze wurden von nun an nicht mehr gezählt. Kleinere und mittlere Infarkte als Folge eines Kathetereingriffs schieden aus der Berechnung aus.
Nicht alle Gruppen folgten sofort dieser Neudefinition. In einer großen Studie aus Amsterdam, die diese neue Zählweise nicht übernommen hatte, fanden sich in der abwartenden Nicht-Eingriffs Gruppe nach einem Jahr 59 Herzinfarkte, in der Katheter-Gruppe 90 Infarkte. Die Autoren fühlten sich veranlasst, ihre Ergebnisse auch nach dem mittlerweile üblichen Kriterium, „größer als 3xULN“, zu berechnen. Dann waren es nicht mehr 90, sondern nur noch 51 Herzinfarkte in der Interventions-Gruppe. Fast die Hälfte der durch Katheter und Stent gesetzten Herzinfarkte war herausgerechnet!
In der AMSTERDAMER-Studie lag die Infarkthäufigkeit als Folge des Katheter-Eingriffs bei 11,3%(!). Seitdem die Schädigungen klein gerechnet werden, gilt der Katheter-Eingriff weltweit als ein äußerst schonender Eingriff.
Das zentrale Resultat der Cochrane-Analyse: Der sofortige reflexhafte Griff zum Herzkatheter bei Verdacht auf Herzinfarkt bietet den Patienten keine substantielle Hilfe. Daraus kann geschlossen werden, dass das kollaterale System bei akuten koronaren Gefäßverschlüssen durchaus wirksam ist.
Ein anschauliches Beispiel ist die erste Sequenz aus dem Film 4: „Vor Stent, nach Stent“: Die Patientin dieses Films kam wegen akuter Herzbeschwerden mit Verdacht auf Herzinfarkt in die Klinik. Dort wurde ihr umgehend ein Katheter gelegt, und per Blick wurde die gezeigte hochgradige Verengung zur „culprit lesion“, zum Übeltäter für die akuten Beschwerden, erklärt. Ihr wurden drei Stents gelegt.
Es war ein länger andauernder Eingriff mit einer enormen Strahlenbelastung. „Vor Stent“ floss das Blut an diesem Engpass vorbei und füllte das Kranzgefäß so, als wenn es dieses Hindernis nicht geben würde. „Nach Stent“ ist die schwere Stenose verschwunden, eine Verbesserung des Blutflusses als dessen Folge ist nicht zu erkennen. Für eine Durchblutungsstörung, und gar eine solche, die einen Herzinfarkt auslöst, gibt es keinen Anhalt. Die kosmetisch eindrucksvolle Beseitigung einer schweren Kranzgefäß-Verengung geriet für die ältere Patientin zu einer heftigen Belastungsprobe. Sie überlebte, brauchte jedoch viele Tage, um sich davon zu erholen.
2017
Alle Studien seit der Mayo-Analyse über COURAGE bis zu ISCHEMIA bestätigten einen günstigen Einfluss von Katheter und Bypass-OP auf die Symptomatik. Patienten mit Brustschmerzen fühlten sich nach den Eingriffen besser als ohne Eingriff. Je ausgeprägter die Schmerzsymptomatik zu Beginn der Studie, desto stärker besserten sich die Symptome nach Stent und Bypass-OP.
Hierzu ist die ORBITA-Studie aus London von 2017 sehr aufschlussreich, in der ein Katheter-Eingriff mit einem Schein-Eingriff verglichen wurde. 200 KHK-Patienten mit einer über 70-%igen Stenose und deutlichen Angina-pektoris-Beschwerden wurden nach Zufallskriterien in zwei Gruppen aufgeteilt. In der einen Gruppe wurde ein Herzkatheter gelegt, die Stenose geweitet und ein Stent eingesetzt. In der anderen Gruppe wurden die Patienten für 15 Minuten schläfrig gemacht, und es wurde ihnen ein Katheter in die Leistenarterie gestochen, jedoch nicht weiter vorgeschoben. Der Katheter wurde nach einiger Zeit wieder entfernt, ohne die Kranzgefäße berührt zu haben. Die Patienten hatten den Eindruck, dass ein kompletter Eingriff stattgefunden habe. Es war ein klassischer Schein-Eingriff.
In den folgenden sechs Wochen kam es zu einer deutlichen Beschwerdelinderung in beiden Gruppen. Angina-pektoris-Beschwerden verschwanden oder waren seltener und die körperliche Belastbarkeit stieg. Der Schein-Eingriff linderte die Beschwerden genauso wie der Katheter-Eingriff plus Stent.
In der Schein-Gruppe kann es nur ein Placeboeffekt gewesen sein. Der Glaube der Patienten, dass sie durch den Hightech-Angriff auf den Gefäßengpass von diesem lebensbedrohlichen Störenfried in ihrem Herzen befreit worden sind, dieser Glaube war die Triebkraft zur Besserung. Wenn der Real-Eingriff an den Kranzgefäßen es nicht besser konnte, dann war auch hier Placebo entscheidend am Werk.
Schon vor ca. 50 Jahren wurden vereinzelt Schein-Operationen am Herzen durchgeführt, die eine Bypass-OP vorgaben. Dabei versah man in Narkose die Haut des Patienten im Bereich des Brustkorbs mit oberflächlichen Schnitten und versorgte diese mit Wund-Klammern. Eindrucksvolle Beschwerdebesserungen wurden berichtet, doch es wurden keine systematischen Studien zu diesem Thema durchgeführt.
ORBITA wird allen Kriterien einer modernen Studie gerecht. Diese Studie beweist, dass die Beschwerdelinderung und die verbesserte körperliche Belastbarkeit durch einen Herzkatheter-Eingriff zu einem entscheidenden Teil ein Placebo-Effekt ist. Hinzu kommt die Betäubung der schmerzleitenden Nerven, die die Kranzarterien umranken, durch den Ballon-Katheter. Die Linderung des Schmerzerlebens, das eine zeitlang anhalten kann, spielt dem Placebo-Effekt in die Hände.
Ein Placebo-Effekt ist bekanntlich umso größer, je größer die Beschwerden und auch je größer der Eingriff – bei einer OP ist er also noch wirksamer als beim Katheter. In den großen Studien zum Katheter und zur OP ist nie von einem Placebo-Effekt die Rede. Die Studienergebnisse werden nie durch die Annahme von Placebo-Effekten relativiert. Placebo-Effekte spielen allerdings eine große Rolle im realen Alltag.
2019
Damit zur letzten Studie, der mit Abstand größten, „ISCHEMIA“. COURAGE erfreute das kardiologische Establishment nicht gerade. Diese Studie wurde solange mit Kritik bedacht, bis eine weitere große Studie auf den Weg gebracht wurde. Damit erschien es erst einmal nicht erforderlich, irgendwelche Konsequenzen aus COURAGE zu ziehen und die Katheter-Frequenzen stiegen weltweit ins Unermessliche.
ISCHEMIA entstand unter der Stabführung des US-amerikanischen Gesundheitsministeriums. Die Vorbereitungen gehen auf das Jahr 2012 zurück. Es geht exakt um den gleichen Ansatz wie bei COURAGE, nur wurden diesmal über 5000 Patienten mit schweren Kranzgefäßveränderungen in 10 kardiologischen Spitzenzentren rund um den Globus einbezogen, in den USA, Sao Paulo, London, Warschau, Bangalore, Guangdong, eine wahrhaft globale Studie. Alle Patienten erhielten eine medikamentöse Therapie, wie sie derzeit den Richtlinien entspricht. Bei 2500, der Hälfte der Patienten, wurde zusätzlich ein Herzkatheter gelegt und anschließend ein Eingriff an den Koronargefäßen durchgeführt. Bei Zweidrittel dieser Patienten wurden Stents gelegt, ein Drittel wurde Bypass-operiert.
Ende 2019 wurden die Ergebnisse auf dem Jahreskongress der American Heart Association vorgestellt. Die Zahl der Todesfälle war nach 3 ½ Jahren Laufzeit in beiden Gruppen absolut identisch. Erneut wurde zweifelsfrei belegt, dass durch Katheter, Stent und Bypass-OP bei schwerer KHK kein Leben gerettet wird.
Die Anzahl der Herzinfarkte zeigte keine signifikanten Unterschiede. In dieser Studie hatte man die Infarkt-Definition noch weiter nach oben verschoben. Bei Stentsetzung waren es >5xULN der CK-MB, bei Bypass-OP >10xULN. Nur wenn der Schädigungs-Indikator das Fünffache bzw. Zehnfache des Normalwerts überschritten hatte, wurde dieser Schaden als das, was er war, als Herzinfarkt, gewertet. Nur die massiven Infarkte wurden in der Interventionsgruppe gezählt, alles andere fiel unter den Tisch. In der Vergleichsgruppe galt wie eh und je die Definition >1xULN, also schlicht das Überschreiten der Obergrenze der CK-MB. So gelang es, Katheter, Stent und Bypass-OP vom Makel hochriskanter Eingriffe zu befreien und als weltweit sehr verträgliche Interventionen hinzustellen.
In den großen Studien werden die Schäden von Herzkatheter und Bypass-OP wegretuschiert. In einer Statistik der AOK – sozusagen als Nachricht aus der realen Welt – hieß es 2014: „0,7% der Patienten verstarben innerhalb von 30 Tagen nach einem Kathetereingriff mit Ballon und Stent“. Bei an die 400.000 Eingriffen pro Jahr eine grauenvolle Bilanz. Die offiziell betriebene Augenwischerei muss dringlich beendet werden. Sowohl die Bypass-OP als auch der angeblich so einfache und ungefährliche Katheter-Eingriff sind mit gravierenden Risiken behaftet.
Die extrem aufwendige ISCHEMIA-Studie – Kosten etwa 100 Millionen Dollar – bringt keine neuen Erkenntnisse. Sie bestätigt lediglich, was seit der Mayo-Analyse und der COURAGE-Studie als Fakt belegt worden war: Katheter, Stent und die Bypass-OP schützen Patienten mit hochgradigen Kranzgefäßverengungen nicht vor einem Herzinfarkt und verlängern ihr Leben nicht.
Auch in ISCHEMIA wird der bekannte Effekt auf die Symptomatik bestätigt. In ersten Stellungnahmen bezogen sich führende US-amerikanische Kardiologen denn auch schwerpunktmäßig darauf, dass Patienten mit Herzbeschwerden, sei es täglich, wöchentlich oder auch nur monatlich, über eine Abnahme ihrer Symptome durch die Eingriffe berichtet hatten. Daraus wurde gefolgert, dass Katheter, Stent und Bypass-OP erste Wahl bleiben bei allen KHK-Patienten mit gelegentlichen Beschwerden. Hauptsache, alles bleibt beim Alten.
Sicher ist eine medikamentöse Behandlung nach den Regeln der Schulmedizin nicht in der Lage, die Herzbeschwerden aller KHK-Patienten zu beseitigen. Das kann jedoch kein Grund sein, zum Katheter zu greifen oder sich einer Bypass-OP zu unterziehen. Das hohe Schadensrisiko dieser Eingriffe wiegt die Beschwerdelinderung, die ja im wesentlichen ein Placebo-Effekt ist, in keiner Weise auf. Und außerdem gibt es wirksame, nicht-eingreifende Mittel und Wege, denen sich die offizielle Medizin verschließt.
Das Fazit der Meilensteine: Katheter und Stent haben sich als wirkungslos erwiesen, das Leben der Patienten zu verlängern und vor einem Herzinfarkt zu schützen. Das gilt bei chronischen belastungsabhängigen Beschwerden, (MAYO, COURAGE, ISCHEMIA), das gilt auch bei akuten Beschwerden und drohendem Herzinfarkt (COCHRANE). Bei bereits eingetretenem Infarkt kann durch den frühzeitigen Katheter-Eingriff kein Leben gerettet werden (US-Register). Die Studien geben insgesamt kein korrektes Bild von den Schäden der koronaren Interventionen. Diese Eingriffe produzieren Infarkte und es kommt zu Todesfällen.
Mittlerweile gibt es über 1000 Herzkatheter-Labore in Deutschland – und die Zahl steigt. Die Katheter-Labore sind ein entscheidender Faktor für das wirtschaftliche Führen eines Krankenhauses geworden. Viele kleine Krankenhäuser, die bei der Bevölkerung wegen ihrer Leistungen und der Betreuung ihrer Patienten geschätzt sind, müssen gegenwärtig in Deutschland schließen, weil sie sich kein Katheter-Labor leisten können.
Die Ärzte und die Gremien, die die Leitlinien zur Behandlung von Herzpatienten formulieren, sind bekannt für ihre Nähe zur Industrie. So ist zu vermuten, dass die Ergebnisse der ISCHEMIA-Studie die Behandlungsvorschriften für Kardiologen und Krankenhäuser nicht wesentlich verändern werden. Der reflexhafte Griff zum Herzkatheter führt gegenwärtig in Deutschland zu 900 000, also fast einer Million Herzkatheter pro Jahr, davon werden in knapp 400 000 Fällen Stents gesetzt. Dazu kommen circa 50 000 Bypass-Operationen.
Die Fachwelt ist mit den Katheter-Aktivitäten eng verwoben. Im Gegensatz zu den Fachleuten könnte eine unbeteiligte Person die ISCHEMIA-Studie als Bankrott-Erklärung von Katheter und Bypass werten. Es wird immens viel Geld bewegt. Ein Katheter-Eingriff mit Stents kostet 5.000 € und mehr, eine Bypass-OP etwa 20.000 €. Die durch Katheter, Stent und Bypass-OP verschleuderten Versichertenbeiträge übersteigen jede fassbare Dimension.
Überfällig: Ein neues Konzept
Warum ist es eigentlich so schwierig, sich eine Durchblutungsstörung im Herzmuskel vorzustellen, die nicht auf einen Verschluss einer Kranzarterie zurückgeht? Fehlt es an Fantasie? Der Grund liegt wohl eher darin, dass in den zurückliegenden Jahrzehnten die Vorstellung vom Kranzgefäß-Verschluss tief in den Köpfen der Menschen verankert wurde und alle anderen Möglichkeiten vom schulmedizinischen System systematisch ausgegrenzt wurden. Der Katheter-Reflex duldet keine Kritik und keine Konkurrenz.
Beim Herz-Echo, der Ultraschall-Untersuchung des Herzens, werden bei Patienten, die unter Herzschmerzen leiden, Störungen in der Beweglichkeit des Herzmuskels gesehen. Während der Systole, der Kontraktion des Herzmuskels, zieht sich nicht die gesamte linke Herzkammer zusammen. In manchen Abschnitten herrscht Stillstand. Hier hat die Herzmuskulatur offenbar an Kraft verloren. Diese Abschnitte werden überdehnt, wodurch die Herzwand in der Schalluntersuchung verschmälert und verdünnt erscheint.
In einem solchen überdehnten Abschnitt herrscht große Spannung. Von dieser Spannung, von diesem Druck, unter dem der gedehnte Muskelabschnitt steht, bekommt man einen anschaulichen Eindruck, wenn man an beiden Enden eines breiten Gummibands, zum Beispiel eines Therabands, kräftig zieht und es damit überdehnt. Im Gegensatz zu einem Gummiband wird der Herzmuskel als lebendiges Gewebe mit Blut, mit Sauerstoff und Nährstoffen versorgt. Wenn der Gewebsdruck aufgrund der Überdehnung immer weiter ansteigt, wird zunehmend die Blutversorgung dieses Muskelabschnitts gestört.
Mit den großen Kranzgefäßen, die der Herzkatheter sichtbar macht, hat das alles nichts zu tun. Es betrifft die zahlreichen Aufzweigungen der Kranzarterien innerhalb der Muskulatur, die durch den Gewebsdruck zunehmend eingeengt werden. Je weiter dieser Prozess fortschreitet, desto mehr werden die Kapillaren, die feinsten Gefäße, die den Sauerstoff an die Zellen leiten, von jeglicher Blutzufuhr abgeschnitten.
Das heißt: Obwohl die großen Kranzgefäße ausreichend Blut heranführen, entsteht eine Mangeldurchblutung im Herzmuskel. Diese Form der Durchblutungsstörung ist Folge der Überdehnung der Muskulatur innerhalb der linken Herzkammer.
Wie kommt es zur Überdehnung? Eine wichtige Ursache für Wandbewegungsstörungen in der linken Herzkammer ist eine Übersäuerung des Herzmuskels. Wie kommt es zu einer Übersäuerung?
Die Lebensrhythmik besteht aus Anspannung und Entspannung. In Anspannungsphasen regiert der Sympathikus, Puls und Blutdruck erhöhen sich, der Herzstoffwechsel wird angetrieben. Dadurch sammeln sich saure Stoffwechselprodukte im Herzen an. Entspannung wird vom Parasympathikus dominiert, der Puls und Blutdruck absenkt, den Herzstoffwechsel bremst und die sauren Stoffwechselprodukte zum Verschwinden bringt.
Ein intakter Parasympathikus schützt das Herz vor Übersäuerung. Wenn der Parasympathikus jedoch länger schwächelt oder gar akut blockiert wird und ausfällt, droht die geschilderte Übersäuerung der linken Herzkammer mit der Folge von Überdehnung und Durchblutungsstörung. Übersäuerung löst Herzschmerzen aus. Bei längerem Anhalten kann Herzmuskelgewebe absterben, womit ein Herzinfarkt entsteht.
Bei KHK-Patienten ist der Parasympathikus in seiner Aktivität eingeschränkt. Ein schwächelnder Parasympathikus ist ein gesichertes Charakteristikum für KHK-Patienten. Es ist gezeigt worden, dass akute Blockaden der parasympathischen Herzimpulse einen Herzanfall auslösen. Der Parasympathikus in seiner Funktion als Herzschutzfaktor ist in diesem Geschehen von elementarer Bedeutung.
Das stellt natürlich die Frage, worunter der Parasympathikus leidet. Die Antwort in aller Kürze: Unter den verschiedenen Faktoren und Einflüssen sind die Luftverschmutzung und die Pestizide in der Nahrung von großer Bedeutung. Stickoxide, „Feinstaub“, also der Dreck in der Luft, und die Nahrungsgifte stimulieren die Bildung sogenannter Radikale im Körper – und diese Radikale schädigen die parasympathischen Nerven nachhaltig. Einseitige Ernährung, Übergewicht, ständiges Sitzen, mangelnder Schlaf sind von Nachteil. Die persönliche Lebensführung ist in der Lage, den Parasympathikus zu stärken oder eben auch zu schwächen. Schwerer Ärger, der kein Ventil findet, ist Gift für den Parasympathikus und nicht selten Auslöser für einen akuten Herzanfall. Die Biologie spielt hinein, denn im Alter lassen die parasympathischen Herzimpulse sukzessive nach.
Eine Durchblutungsstörung als Folge von Übersäuerung und Überdehnung geht auf verschiedenste Ursachen zurück und hat nichts mit den Kranzgefäßen zu tun. Neben dem Parasympathikus gibt es weitere wichtige Schutzfaktoren des Herzens: Signalstoffe wie NO (Stickstoffmonoxid), bestimmte Vitamine und Hormone. Alle Schutzfaktoren zusammen erfreuen sich, wenn sich Körper, Geist und Seele einigermaßen im Gleichgewicht befinden, wenn die Stickoxide aus der Luft und Glyphosat aus der Nahrung verschwinden würde. Ein weites Feld. An anderer Stelle habe ich mich ausführlich zu diesem gesamten Themenkomplex geäußert, s. Literaturhinweise.
Strophanthin – ein Hoffnungsträger
Es gibt Medikamente, die die Herzschutzfaktoren anregen und kräftigen. Allen voran ist Strophanthin zu nennen, eine Substanz, die aus den Samen einer afrikanischen Liane gewonnen wird.
Strophanthin war über 50 Jahre in Deutschland das Mittel zur Behandlung von Patienten mit Herzschwäche und Angina pektoris. Mit Aufkommen der Beta-Blocker und ACE-Hemmer gegen Ende des Jahrhunderts wurde Strophanthin an den Rand gedrängt und aus dem schulmedizinischen Repertoire ausgegrenzt.
Wer als Arzt häufig Strophanthin einsetzt, hält dieses Mittel für einen Glücksfall für Herzkranke. Ein Patient, der über Herzanfälle klagt, erlebt sehr bald, dass seine Anfälle zurückgehen. Patienten mit Herzschwäche kommen nach einiger Zeit die Treppen wieder besser hoch. Mit Strophanthin werden die Patienten in der Regel ruhiger, gelassener, viele schlafen besser. Ein Herzpatient, dem Strophanthin verschrieben wurde, will davon in der Regel nicht mehr lassen.
Warum? In niedriger Dosis stärkt Strophanthin den Parasympathikus und weitere Herzschutzfaktoren und aktiviert innerhalb der Herzmuskelzelle verschiedene Signalwege mit protektiven Effekten. Strophanthin schützt den Herzmuskel vor Übersäuerung und Angina pektoris. Ein geschwächter Herzmuskel wird durch Strophanthin in seiner Kontraktionskraft unterstützt. Dazu schützt Strophanthin vor Rhythmusstörungen des Herzens. Dies alles ist belegt. Strophanthin ist von kräftiger Wirkung, wenn die verschiedenen Funktionen des Herzens aus dem Tritt geraten sind. In erster Linie stimuliert es körpereigene Regulationsvorgänge, wenn diese abgeschwächt sind. Am gesunden Herzen hat es hingegen kaum einen Effekt.
Dazu kommt: Im Gegensatz zu den heute üblichen Herzmedikamenten ist Strophanthin bei oraler Anwendung praktisch frei von Nebenwirkungen. Eine mögliche Anregung der Darmtätigkeit wird im Allgemeinen gern akzeptiert, Durchfall ist sehr selten und lässt sich durch Verminderung der eingenommenen Dosis beheben. Das Nebenwirkungs- und Schädigungsspektrum von ASS, Statinen, ACE-Hemmern oder Beta-Blockern ist im Vergleich von anderem ganz anderen Kaliber.
Wie oft bei Naturprodukten, hängt die Art der Wirksamkeit auch beim Strophanthin davon ab, ob man niedrig oder hoch dosiert. Strophanthin entfaltet seine segensreichen Wirkungen im Niedrigdosis-Bereich, im Hochdosis-Bereich ist es schnell toxisch. Von schulmedizinischer Seite hat man Strophanthin mit Digitalis, den Fingerhut-Präparaten, die in üblicher Dosierung schnell giftig wirken, in einen Topf geworfen. Damit hat man von offizieller Seite nur den toxischen Wirkungsbereich zur Kenntnis genommen und bestreitet die Wirkungen von Strophanthin im Niedrigdosis-Bereich.
Wenn ein Patient heutzutage das Wort Strophanthin gegenüber einem Arzt erwähnt, stößt er in der Regel nur auf Ablehnung. Das Einzige, was dem schulmedizinisch tätigen Arzt vom Strophanthin bekannt ist, ist die Hemmung der sogenannten Natriumpumpe, ein Effekt, der auch in der Forschung vielfach verwendet wird. Hierbei werden Dosierungen im toxischen Hochdosisbereich benutzt.
Anfang der Neunziger Jahre wurde vermutet, dass Strophanthin auch ein menschliches Hormon sei, das in der Nebenniere produziert wird. Die dadurch ausgelöste Forschungstätigkeit ergab unter anderem, dass Strophanthin in niedriger Dosierung genannte Pumpe nicht hemmt, sondern aktiviert. Vor allem ist deutlich geworden, dass Strophanthin den gesamten Stoffwechsel der Herzmuskelzellen stimuliert und über die Aktivierung verschiedener Signalkaskaden vielfältige protektive Effekte im Herzmuskel auslöst. Die umfassenden Erkenntnisse der letzten 20 – 25 Jahre sind leider völlig unbeachtet an der Schulmedizin vorbeigegangen.
Der subjektive Eindruck von Arzt und Patient beweist keine objektiv bestehenden Wirkungen. Überfällig sind „evidenz-basierte“ Studien, Strophanthin gegen Placebo bei KHK-Patienten und bei Patienten mit Herzschwäche. Das Scheitern von Katheter, Stent und Bypass und die mit diesen Eingriffen nutzlos ausgegebenen Milliarden sollten zumindest für die Patienten und die Kostenträger Anlass genug sein, eine Zulassungsstudie für Strophanthin auf den Weg zu bringen.
Um zwei solche Studien kurz zu skizzieren: In die KHK-Studie sollte die gleiche Klientel eingeschlossen werden wie bei COURAGE und ISCHEMIA, Patienten mit Angina-pektoris-Beschwerden unter Belastung. Nach einer Behandlungsdauer mit Strophanthin von 6 bzw. 12 Wochen wäre die physische Leistungsfähigkeit zu kontrollieren und der jeweilige Status der anginösen Herzbeschwerden zu erfassen. Zu Beginn der Studie und nach Abschluss der Behandlung sollte ein Belastungs-Szintigramm des Herzmuskels durchgeführt werden.
Ein Szintigramm ermöglicht es, Durchblutungsstörungen im Herzmuskel sichtbar zu machen. Mangelnde Blutzufuhr ist der Auslöser von Angina pektoris und Herzinfarkt. Indem Strophanthin den Herzmuskel vor Übersäuerung schützt, verhindert es, dass die Muskulatur überdehnt wird und darüber die Blutversorgung des Herzens behindert wird. Der Schutz vor Übersäuerung ist ein Schutz vor Durchblutungsstörungen.
Es käme auf den Vergleich der Szintigramme vor Strophanthin-Behandlung und nach 6 oder 12 Wochen an. Eine verbesserte Durchblutung des Herzmuskels nach wenigen Wochen wäre ein gewichtiges Argument für Strophanthin. Dabei ist an Zerbeiß-Kapseln oder eine Tinktur gedacht, deren Wirkstoff über die Zunge aufgenommen bzw. geschluckt und über den Darm resorbiert wird.
In einer Studie an Patienten mit Herzschwäche, auch ausgeprägter Herzschwäche, sollte die im Einzelfall immer wieder zu beobachtende Leistungssteigerung durch Strophanthin objektiv abgeklärt werden.
Bei diesen beiden umgrenzten Studien sollte man mit einem minimalen Bruchteil dessen auskommen, was in ISCHEMIA investiert worden ist. Natürlich braucht es dafür eine mutige Klinik. Die pharmazeutische Industrie ist nicht interessiert an einem Naturstoff, der nicht patentierbar ist und deshalb nicht beliebig profitabel vermarktet werden kann. Also braucht es mutige Sponsoren.
Ein Schritt weiter: Da Strophanthin bei einem Herzinfarkt experimentell nachweislich die Übersäuerung des Herzmuskels drastisch zurückdrängt, sollte Strophanthin dringlich bei akuten Herzsymptomen, speziell auch bei drohendem Herzinfarkt eingesetzt werden. Bei eingetretenem Herzinfarkt kann durch Strophanthin lebensbedrohlichen Komplikationen durch die Verminderung der Übersäuerung und durch die Aktivierung schützender Signalweg in den Herzmuskelzellen entgegengewirkt werden. Deshalb: Statt umgehend zum Herzkatheter zu greifen, sollte sofort Strophanthin gegeben werden, wie dies in manchen deutschen Kliniken bis in die Siebziger Jahre erfolgreich praktiziert worden ist.
Der ökonomische Druck ist riesig. Theorie und Praxis werden gegen jegliche Einwände abgeschottet. Es mutet an wie Denksperren, wenn sich die Schulmedizin dem kollateralen System oder dem Strophanthin gegenüber verschließt. In den Medien wird man nicht müde, auf die in den Kranzgefäßen lauernde Gefahr hinzuweisen, der angeblich nur mit Katheter, Stent und Bypass-OP beizukommen ist.
Doch die Patienten haben ein Anrecht auf korrekte Information. Und sie haben ein Anrecht darauf, dass realistische neue therapeutische Wege fachgerecht geprüft werden. Wenn sich die Industrie dem Strophanthin gegenüber verweigert, sind Staat und Gesellschaft gefragt. Strophanthin-Studien dürften gern im Auftrag des Gesundheitsministeriums oder auch im Rahmen der deutschen Herzstiftung erfolgen. Dazu braucht es Druck von Seiten der Öffentlichkeit, von Patienten, von kritischen Ärzten, von Seiten der Medien und der Politik. Es braucht dringlich Druck von Seiten der Kostenträger, denn schließlich wird alles von den Versicherten bezahlt. Das Thema muss in die öffentliche Diskussion, wenn sich etwas ändern soll.
Dr. Knut Sroka
Arzt für Allgemeinmedizin
Hamburg, Mai 2020
Ich danke allen meinen Patienten, die mir ihre Katheter-Filme zur Verfügung gestellt und mir erlaubt haben, sie im Rahmen dieses Arbeitsprojekts zu verwenden.
Und ich danke Prof. W. J. Huk, Erlangen, für die intensive Diskussion, die wir über die verschiedensten inhaltlichen Aspekte dieser Arbeit geführt haben.
LITERATURHINWEISE
ANATOMIE:
– Baroldi G u.a.: The Collaterals of the Coronary Arteries in Normal and Pathologic Hearts. Circ Res 1956; 4:223-22
– Baroldi G: Coronary stenosis: Ischemic or non-ischemic factor? Am Heart J 1978; 96:139-143
– Baroldi G: Coronary thrombosis: Facts and beliefs. Am Heart J 1976; 91:683-688
STUDIEN:
FAMA II:
De Bruyne B, Fearon WF, Pijls NH, et al.: Fractional flow reserve-guided PCI for stable coronary artery disease. N Engl J Med 2014; 371: 1208–17
MAYO-Clinic:
Rihal CS u.a.: Indications for coronary artery bypass surgery and percutaneous coronary intervention in chronic stable angina. Circulation 2003; 108:2439-2445
COURAGE:
– Boden WE u.a.: COURAGE Trial Group: Optimal medical therapy with or without PCI for stable coronary disease. N Engl J Med 2007; 356:1503-1516
– Sedlis SP, Hartigan PM, Teo KK, et al.: Effect of PCI on long-term survival in patients with stable ischemic heart disease. N Engl J Med 2015; 373: 1937–46
COCHRANE-Analysis:
Routine invasive strategies versus selective invasive strategies for unstable angina and non-ST elevation myocardial infarction in the stent era. Cochrane Database Syst Rev 2016; May 26;(5):CD004815
US-Herzkatheter-Register:
Menees DS u.a.: Door-to-Balloon Time and Mortality among Patients Ungergoing Primary PCI. N Engl J Med 2013; 369:901-909
AMSTERDAM:
de Winter RJ u.a.: Invasive versus Conservative Treatment in Unstable Coronary Syndromes (ICTUS) Investigators. N Engl J Med 2005; 353:1095-1110
ORBITA:
Al-Lamee R u.a.: Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. Lancet 2017; DOI: http://dx.doi.org/10.1016/S0140-6736(17)32714-9
ISCHEMIA:
– Hochman JS, Reynolds HR, Bangalore S, et al.: Baseline characteristics and risk profiles of participants in the ISCHEMIA randomized clinical trial. JAMA cardiology 2019; 4: 273–86
– Hochman J: ISCHEMIA trial: primary report of clinical outcomes. Presentation at the American Heart Association Meeting, Philadelphia, November 2019. 2019
NEUES KONZEPT:
Literatur s. Sroka K: Herzinfarkt – Alternativen zu Bypass, Stent und Herzkatheter. VAK-Verlag, Kirchzarten bei Freiburg, 2019
STROPHANTHIN:
Sroka K: Strophanthin – Eine Neubewertung. Med Welt 2015; 66:275–280. (Auf der Website www.herzinfarkt-alternativen.de abgelegt)